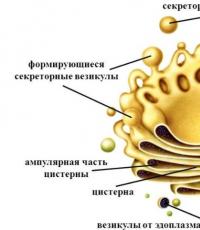
Какие реакции называют реакциями обмена. Классификация химических реакций
9.1. Какие бывают химические реакции
Вспомним, что химическими реакциями мы называем любые химические явления природы. При химической реакции происходит разрыв одних и образование других химических связей. В результате реакции из одних химических веществ получаются другие вещества (см. гл. 1).
Выполняя домашнее задание к § 2.5, вы познакомились с традиционным выделением из всего множества химических превращений реакций четырех основных типов, тогда же вы предложили и их названия: реакции соединения, разложения, замещения и обмена.
Примеры реакций соединения:
C + O 2 = CO 2 ; (1)
Na 2 O + CO 2 = Na 2 CO 3 ; (2)
NH 3 + CO 2 + H 2 O = NH 4 HCO 3 . (3)
Примеры реакций разложения:
2Ag 2 O 4Ag + O 2 ; (4)
CaCO 3
CaO + CO 2 ; (5)
(NH 4) 2 Cr 2 O 7 N 2 + Cr 2 O 3 +
4H 2 O . (6)
Примеры реакций замещения:
CuSO 4 + Fe = FeSO 4 + Cu ; (7)
2NaI + Cl 2 = 2NaCl + I 2 ; (8)
CaCO 3 + SiO 2 = CaSiO 3 + CO 2 . (9)
| Реакции обмена – химические реакции, в которых исходные вещества как бы обмениваются своими составными частями. |
Примеры реакций обмена:
Ba(OH) 2 + H 2 SO 4 = BaSO 4 + 2H 2 O;
(10)
HCl + KNO 2 = KCl + HNO 2 ; (11)
AgNO 3 + NaCl = AgCl + NaNO 3 . (12)
Традиционная классификация
химических реакций не охватывает все их
разнообразие – кроме реакций четырех основных
типов существует еще и множество более сложных
реакций.
Выделение двух других типов химических реакций
основано на участии в них двух важнейших
нехимических частиц: электрона и протона.
При протекании некоторых реакций происходит
полная или частичная передача электронов от
одних атомов к другим. При этом степени окисления
атомов элементов, входящих в состав исходных
веществ, изменяются; из приведенных примеров это
реакции 1, 4, 6, 7 и 8. Эти реакции называются окислительно-восстановительными
.
В другой группе реакций от одной реагирующей частицы к другой переходит ион водорода (Н +), то есть протон. Такие реакции называют кислотно-основными реакциями или реакциями с передачей протона .
Среди приведенных примеров такими реакциями являются реакции 3, 10 и 11. По аналогии с этими реакциями окислительно-восстановительные реакции иногда называют реакциями с передачей электрона . С ОВР вы познакомитесь в § 2, а с КОР – в следующих главах.
РЕАКЦИИ СОЕДИНЕНИЯ,
РЕАКЦИИ РАЗЛОЖЕНИЯ, РЕАКЦИИ ЗАМЕЩЕНИЯ, РЕАКЦИИ
ОБМЕНА, ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ,
КИСЛОТНО-ОСНОВНЫЕ РЕАКЦИИ.
Составьте
уравнения реакций, соответствующих следующим
схемам:
а) HgO Hg + O 2 (t
); б) Li 2 O
+ SO 2
Li 2 SO 3 ; в) Cu(OH) 2 CuO + H 2 O (t
);
г) Al + I 2 AlI 3 ; д) CuCl 2 + Fe FeCl 2 + Cu; е) Mg + H 3 PO 4
Мg 3 (PO 4) 2
+ H 2 ;
ж) Al + O 2 Al 2 O 3 (t
); и) KClO 3
+ P P 2 O 5
+ KCl (t
); к) CuSO 4 + Al Al 2 (SO 4) 3 + Cu;
л) Fe + Cl 2 FeCl 3 (t
); м) NH 3 + O 2 N 2 +
H 2 O (t
); н) H 2 SO 4 + CuO CuSO 4 + H 2 O.
Укажите традиционный тип реакции. Отметьте
окислительно-восстановительные и
кислотно-основные реакции. В
окислительно-восстановительных реакциях
укажите, атомы каких элементов меняют свои
степени окисления.
9.2. Окислительно-восстановительные реакции
Рассмотрим окислительно-восстановительную реакцию, протекающую в доменных печах при промышленном получении железа (точнее, чугуна) из железной руды:
Fe 2 O 3 + 3CO = 2Fe + 3CO 2 .
Определим степени окисления атомов, входящих в состав как исходных веществ, так и продуктов реакции
| Fe 2 O 3 | + | = | 2Fe | + |
Как видите, степень окисления атомов углерода в результате реакции увеличилась, степень окисления атомов железа уменьшилась, а степень окисления атомов кислорода осталась неизменной. Следовательно, атомы углерода в этой реакции подверглись окислению, то есть потеряли электроны (окислились ), а атомы железа – восстановлению, то есть присоединили электроны (восстановились ) (см. § 7.16). Для характеристики ОВР используют понятия окислитель и восстановитель .

Таким образом, в нашей реакции атомами-окислителями являются атомы железа, а атомами-восстановителями – атомы углерода.
В нашей реакции веществом-окислителем
является оксид железа(III), а
веществом-восстановителем – оксид углерода(II).
В тех случаях, когда атомы-окислители и
атомы-восстановители входят в состав одного и
того же вещества (пример: реакция 6 из предыдущего
параграфа), понятия " вещество-окислитель" и
" вещество-восстановитель" не используются.
Таким образом, типичными окислителями являются
вещества, в состав которых входят атомы, склонные
присоединять электроны (полностью или частично),
понижая свою степень окисления. Из простых
веществ это прежде всего галогены и кислород, в
меньшей степени сера и азот. Из сложных веществ –
вещества, в состав которых входят атомы в высших
степенях окисления, не склонные в этих степенях
окисления образовывать простые ионы: HNO 3 (N +V),
KMnO 4 (Mn +VII), CrO 3 (Cr +VI), KClO 3
(Cl +V), KClO 4 (Cl +VII) и др.
Типичными восстановителями являются вещества, в
состав которых входят атомы, склонные полностью
или частично отдавать электроны, повышая свою
степень окисления. Из простых веществ это
водород, щелочные и щелочноземельные металлы, а
также алюминий. Из сложных веществ – H 2 S и
сульфиды (S –II), SO 2 и сульфиты (S +IV),
йодиды (I –I), CO (C +II), NH 3 (N –III)
и др.
В общем случае почти все сложные и многие простые
вещества могут проявлять как окислительные, так
и восстановительные свойства. Например:
SO 2 + Cl 2 = S + Cl 2 O 2 (SO 2 –
сильный восстановитель);
SO 2 + C = S + CO 2 (t) (SO 2 – слабый
окислитель);
C + O 2 = CO 2 (t) (C – восстановитель);
C + 2Ca = Ca 2 C (t) (С – окислитель).
Вернемся к реакции, разобранной нами в начале
этого параграфа.
| Fe 2 O 3 | + | = | 2Fe | + |
Обратите внимание, что в результате реакции атомы-окислители (Fe +III) превратились в атомы-восстановители (Fe 0), а атомы-восстановители (C +II) превратились в атомы-окислители (C +IV). Но CO 2 в любых условиях очень слабый окислитель, а железо, хоть и является восстановителем, но в данных условиях значительно более слабым, чем CO. Поэтому продукты реакции не реагируют друг с другом, и обратная реакция не протекает. Приведенный пример является иллюстрацией общего принципа, определяющего направление протекания ОВР:
Окислительно-восстановительные реакции протекают в направлении образования более слабого окислителя и более слабого восстановителя.
Окислительно-восстановительные
свойства веществ можно сравнивать только в
одинаковых условиях. В некоторых случаях это
сравнение может быть проведено количественно.
Выполняя домашнее задание к первому параграфу
этой главы, вы убедились, что подобрать
коэффициенты в некоторых уравнениях реакций
(особенно ОВР) довольно сложно. Для упрощения
этой задачи в случае
окислительно-восстановительных реакций
используют следующие два метода:
а) метод электронного баланса
и
б) метод электронно-ионного баланса
.
Метод электронного баланса вы изучите сейчас, а
метод электронно-ионного баланса обычно
изучается в высших учебных заведениях.
Оба эти метода основаны на том, что электроны в
химических реакциях никуда не исчезают и
ниоткуда не появляются, то есть число принятых
атомами электронов равно числу электронов,
отданных другими атомами.
Число отданных и принятых электронов в методе
электронного баланса определяется по изменению
степени окисления атомов. При использовании
этого метода необходимо знать состав как
исходных веществ, так и продуктов реакции.
Рассмотрим применение метода электронного
баланса на примерах.
Пример 1. Составим уравнение реакции железа с хлором. Известно, что продуктом такой реакции является хлорид железа(III). Запишем схему реакции:
Fe + Cl 2 FeCl 3 .
Определим степени окисления атомов всех элементов, входящих в состав веществ, участвующих в реакции:
Атомы железа отдают электроны, а
молекулы хлора их принимают. Выразим эти
процессы электронными уравнениями
:
Fe – 3e
– = Fe +III ,
Cl 2 + 2e –
= 2Cl –I .
Чтобы число отданных электронов было равно числу принятых, надо первое электронное уравнение умножить на два, а второе – на три:
| Fe – 3e
– = Fe +III , Cl 2 + 2e – = 2Cl –I |
2Fe – 6e
– = 2Fe +III , 3Cl 2 + 6e – = 6Cl –I . |
Введя коэффициенты 2 и 3 в схему
реакции, получаем уравнение реакции:
2Fe + 3Cl 2 = 2FeCl 3 .
Пример 2. Составим уравнение реакции горения белого фосфора в избытке хлора. Известно, что в этих условиях образуется хлорид фосфора(V):
| +V –I | ||||
| P 4 | + | Cl 2 | PCl 5 . |
Молекулы белого фосфора отдают электроны (окисляются), а молекулы хлора их принимают (восстанавливаются):
| P 4 – 20e
– = 4P +V Cl 2 + 2e – = 2Cl –I |
1 10 |
2 20 |
P 4 – 20e
– = 4P +V Cl 2 + 2e – = 2Cl –I |
P 4 – 20e
– = 4P +V 10Cl 2 + 20e – = 20Cl –I |
Полученные первоначально множители (2 и 20) имели общий делитель, на который (как будущие коэффициенты в уравнении реакции) и были разделены. Уравнение реакции:
P 4 + 10Cl 2 = 4PCl 5 .
Пример 3. Составим уравнение реакции, протекающей при обжиге сульфида железа(II) в кислороде.
Схема реакции:
| +III –II | +IV –II | |||||
| + | O 2 | + |
В этом случае окисляются и атомы
железа(II), и атомы серы(– II). В состав сульфида
железа(II) атомы этих элементов входят в отношении
1:1 (см. индексы в простейшей формуле).
Электронный баланс:
| 4 | Fe +II – e
– = Fe +III S –II – 6e – = S +IV |
Всего отдают 7е – |
| 7 | O 2 + 4e – = 2O –II |
Уравнение реакции: 4FeS + 7O 2 = 2Fe 2 O 3 + 4SO 2 .
Пример 4 . Составим уравнение реакции, протекающей при обжиге дисульфида железа(II) (пирита) в кислороде.
Схема реакции:
| +III –II | +IV –II | |||||
| + | O 2 | + |
Как и в предыдущем примере, здесь тоже окисляются и атомы железа(II), и атомы серы, но со степенью окисления – I. В состав пирита атомы этих элементов входят в отношении 1:2 (см. индексы в простейшей формуле). Именно в этом отношении атомы железа и серы вступают в реакцию, что и учитывается при составлении электронного баланса:
| Fe +III – e
– = Fe +III 2S –I – 10e – = 2S +IV |
Всего отдают 11е – | |
| O 2 + 4e – = 2O –II |
Уравнение реакции: 4FeS 2 + 11O 2 = 2Fe 2 O 3 + 8SO 2 .
Встречаются и более сложные случаи ОВР, с некоторыми из них вы познакомитесь, выполняя домашнее задание.
АТОМ-ОКИСЛИТЕЛЬ,
АТОМ-ВОССТАНОВИТЕЛЬ, ВЕЩЕСТВО-ОКИСЛИТЕЛЬ,
ВЕЩЕСТВО-ВОССТАНОВИТЕЛЬ, МЕТОД ЭЛЕКТРОННОГО
БАЛАНСА, ЭЛЕКТРОННЫЕ УРАВНЕНИЯ.
1.Составьте
электронный баланс к каждому уравнению ОВР,
приведенному в тексте § 1 этой главы.
2.Составьте уравнения ОВР, обнаруженных вами при
выполнении задания к § 1 этой главы. На этот раз
для расстановки коэффициентов используйте метод
электронного баланса. 3.Используя метод
электронного баланса, составьте уравнения
реакций, соответствующие следующим схемам: а) Na + I 2
NaI;
б) Na + O 2 Na 2 O 2 ;
в) Na 2 O 2 + Na Na 2 O;
г) Al + Br 2 AlBr 3 ;
д) Fe + O 2 Fe 3 O 4 (t
);
е) Fe 3 O 4 + H 2 FeO + H 2 O (t
);
ж) FeO + O 2 Fe 2 O 3 (t
);
и) Fe 2 O 3 + CO Fe + CO 2 (t
);
к) Cr + O 2 Cr 2 O 3 (t
);
л) CrO 3 + NH 3 Cr 2 O 3 + H 2 O + N 2
(t
);
м) Mn 2 O 7 + NH 3 MnO 2 + N 2 + H 2 O;
н) MnO 2 + H 2 Mn + H 2 O (t
);
п) MnS + O 2 MnO 2 + SO 2 (t
)
р) PbO 2 + CO Pb + CO 2 (t
);
с) Cu 2 O + Cu 2 S Cu + SO 2 (t
);
т) CuS + O 2 Cu 2 O +SO 2 (t
);
у) Pb 3 O 4 + H 2 Pb + H 2 O (t
).
9.3. Экзотермические реакции. Энтальпия
Почему происходят химические реакции?
Для ответа на этот вопрос вспомним, почему
отдельные атомы объединяются в молекулы, почему
из изолированных ионов образуется ионный
кристалл, почему при образовании электронной
оболочки атома действует принцип наименьшей
энергии. Ответ на все эти вопросы один и тот же:
потому, что это энергетически выгодно. Это
значит, что при протекании таких процессов
выделяется энергия. Казалось бы, что и химические
реакции должны протекать по этой же причине.
Действительно, можно провести множество реакций,
при протекании которых выделяется энергия.
Энергия выделяется, как правило, в виде теплоты.
Если при экзотермической реакции
теплота не успевает отводиться, то реакционная
система нагревается.
Например, в реакции горения метана
СН 4(г) + 2О 2(г) = СО 2(г) + 2Н 2 О (г)
выделяется столько теплоты, что метан
используется как топливо.
Тот факт, что в этой реакции выделяется теплота,
можно отразить в уравнении реакции:
СН 4(г) + 2О 2(г) = СО 2(г) + 2Н 2 О (г) + Q.
Это так называемое термохимическое
уравнение
. Здесь символ "+Q
" означает,
что при сжигании метана выделяется теплота. Эта
теплота называется тепловым эффектом реакции
.
Откуда же берется выделяющаяся теплота?
Вы знаете, что при химических реакциях рвутся и
образуются химические связи. В данном случае
рвутся связи между атомами углерода и водорода в
молекулах СН 4 , а также между атомами
кислорода в молекулах О 2 . При этом
образуются новые связи: между атомами углерода и
кислорода в молекулах СО 2 и между атомами
кислорода и водорода в молекулах Н 2 О. Для
разрыва связей нужно затратить энергию (см.
"энергия связи" , "энергия атомизации"),
а при образовании связей энергия выделяется.
Очевидно, что, если "новые" связи более
прочные, чем "старые" , то энергии выделится
больше, чем поглотится. Разность между
выделившейся и поглощенной энергией и
составляет тепловой эффект реакции.
Тепловой эффект (количество теплоты) измеряется
в килоджоулях, например:
2Н 2(г) + О 2(г) = 2Н 2 О (г) + 484 кДж.
Такая запись означает, что 484 килоджоуля теплоты выделится, если два моля водорода прореагируют с одним молем кислорода и при этом образуется два моля газообразной воды (водяного пара).
Таким образом, в термохимических уравнениях коэффициенты численно равны количествам вещества реагентов и продуктов реакции .
От чего зависит тепловой эффект каждой
конкретной реакции?
Тепловой эффект реакции зависит
а) от агрегатных состояний исходных веществ и
продуктов реакции,
б) от температуры и
в) от того, происходит ли химическое превращение
при постоянном объеме или при постоянном
давлении.
Зависимость теплового эффекта реакции от
агрегатного состояния веществ связана с тем, что
процессы перехода из одного агрегатного
состояния в другое (как и некоторые другие
физические процессы) сопровождаются выделением
или поглощением теплоты. Это также может быть
выражено термохимическим уравнением. Пример –
термохимическое уравнение конденсации водяного
пара:
Н 2 О (г) = Н 2 О (ж) + Q.
В термохимических уравнениях, а при
необходимости и в обычных химических уравнениях,
агрегатные состояния веществ указываются с
помощью буквенных индексов:
(г) – газ,
(ж) – жидкость,
(т) или (кр) – твердое или кристаллическое
вещество.
Зависимость теплового эффекта от температуры
связана с различиями в теплоемкостях
исходных
веществ и продуктов реакции.
Так как в результате экзотермической реакции при
постоянном давлении всегда увеличивается объем
системы, то часть энергии уходит на совершение
работы по увеличению объема, и выделяющаяся
теплота будет меньше, чем в случае протекания той
же реакции при постоянном объеме.
Тепловые эффекты реакций обычно рассчитывают
для реакций, протекающих при постоянном объеме
при 25 ° С и обозначают символом Q
o .
Если энергия выделяется только в виде теплоты, а
химическая реакция протекает при постоянном
объеме, то тепловой эффект реакции (Q V
)
равен изменению внутренней энергии
(D U
)
веществ-участников реакции, но с противоположным
знаком:
Q V = – U .
Под внутренней энергией тела понимают суммарную энергию межмолекулярных взаимодействий, химических связей, энергию ионизации всех электронов, энергию связей нуклонов в ядрах и все прочие известные и неизвестные виды энергии, " запасенные" этим телом. Знак " – " обусловлен тем, что при выделении теплоты внутренняя энергия уменьшается. То есть
U = – Q V .
Если же реакция протекает при постоянном давлении, то объем системы может изменяться. На совершение работы по увеличению объема также уходит часть внутренней энергии. В этом случае
U = – (Q P + A ) = –(Q P + P V ),
где Q p – тепловой эффект реакции, протекающей при постоянном давлении. Отсюда
Q P = – U – P V .
Величина, равная U + P V получила название изменение энтальпии и обозначается D H .
H = U + P V .
Следовательно
Q P = – H .
Таким образом, при выделении теплоты
энтальпия системы уменьшается. Отсюда старое
название этой величины: " теплосодержание" .
В отличие от теплового эффекта, изменение
энтальпии характеризует реакцию независимо от
того, протекает она при постоянном объеме или
постоянном давлении. Термохимические уравнения,
записанные с использованием изменения
энтальпии, называются термохимическими
уравнениями в термодинамической форме
. При
этом приводится значение изменения энтальпии в
стандартных условиях (25 °С, 101,3 кПа), обозначаемое H о
. Например:
2Н 2(г) + О 2(г) = 2Н 2 О (г) H о
= – 484 кДж;
CaO (кр) + H 2 O (ж) = Сa(OH) 2(кр) H о
= – 65 кДж.
Зависимость количества теплоты, выделяющейся в реакции (Q ) от теплового эффекта реакции (Q o) и количества вещества (n Б) одного из участников реакции (вещества Б – исходного вещества или продукта реакции) выражается уравнением:
Здесь Б – количество вещества Б, задаваемое коэффициентом перед формулой вещества Б в термохимическом уравнении.
Задача
Определите количество вещества водорода, сгоревшего в кислороде, если при этом выделилось 1694 кДж теплоты.
Решение
2Н 2(г) + О 2(г) = 2Н 2 О (г) + 484 кДж. |
|
|
Q = 1694 кДж,
6.Тепловой эффект реакции взаимодействия
кристаллического алюминия с газообразным хлором
равен 1408 кДж. Запишите термохимическое уравнение
этой реакции и определите массу алюминия,
необходимого для получения 2816 кДж теплоты с
использованием этой реакции. 9.4. Эндотермические реакции. Энтропия Кроме экзотермических реакций возможны реакции, при протекании которых теплота поглощается, и, если ее не подводить, то реакционная система охлаждается. Такие реакции называют эндотермическими . Тепловой эффект таких реакций
отрицательный. Например: Таким образом, энергия, выделяющаяся
при образовании связей в продуктах этих и им
подобных реакций, меньше, чем энергия,
необходимая для разрыва связей в исходных
веществах.
Возьмем две колбы и заполним одну из
них азотом (бесцветный газ), а другую – диоксидом
азота (бурый газ) так, чтобы и давление, и
температура в колбах были одинаковыми. Известно,
что эти вещества между собой не вступают в
химическую реакцию. Герметично соединим колбы
горлышками и установим их вертикально, так, чтобы
колба с более тяжелым диоксидом азота была внизу
(рис. 9.1). Через некоторое время мы увидим, что
бурый диоксид азота постепенно распространяется
в верхнюю колбу, а бесцветный азот проникает в
нижнюю. В результате газы смешиваются, и окраска
содержимого колб становится одинаковой. Таким образом,
Уравнения связи между энтропией (S
)
и другими величинами изучаются в курсах физики и
физической химии. Единица измерений энтропии [S
]
= 1 Дж/К. G = H – T S Условие самопроизвольного протекания реакции: G < 0. При низких температурах фактором, определяющим возможность протекания реакции в большей степени является энергетический фактор, а при высокой – энтропийный. Из приведенного уравнения, в частности, видно, почему не протекающие при комнатной температуре реакции разложения (энтропия увеличивается) начинают идти при повышенной температуре. ЭНДОТЕРМИЧЕСКАЯ
РЕАКЦИЯ, ЭНТРОПИЯ, ЭНЕРГЕТИЧЕСКИЙ ФАКТОР,
ЭНТРОПИЙНЫЙ ФАКТОР, ЭНЕРГИЯ ГИББСА.
2CuO (кр) + C (графит) = 2Cu (кр) + CO 2(г) составляет –46 кДж. Запишите
термохимическое уравнение и рассчитайте, какую
энергию нужно затратить для получения 1 кг меди
по такой реакции. CaCO 3(кр) = CaO (кр) + CO 2(г) – 179кДж образовалось 24,6 л углекислого газа.
Определите, какое количество теплоты было
израсходовано бесполезно. Сколько граммов
оксида кальция при этом образовалось? |
Познакомимся с последним типом реакций по признаку «число и состав исходных веществ и продуктов реакции».
В демонстрационную пробирку нальём раствор щёлочи - гидроксида натрия, а затем добавим к нему раствор соли - сульфата меди (II). Выпадет густой синий осадок нерастворимого в воде гидроксида меди (II) (рис. 108). Если небольшую часть содержимого из пробирки, в которой образовался осадок, профильтровать и выпарить несколько капель полученного раствора на часовом стекле, то нетрудно будет заметить появление белых кристалликов соли, образовавшейся в ходе реакции:

Рис. 108. Взаимодействие гидроксида натрия с сульфатом меди (II)
Чтобы подчеркнуть, что в результате реакции образуется осадок нерастворимого в воде гидроксида меди (II), рядом с его формулой в уравнении реакции записывают стрелку, направленную вниз.
Бесспорно, полученная соль может быть только сульфатом натрия Na 2 SО 4:
В результате проведённой реакции два сложных вещества ионного строения - гидроксид натрия и сульфат меди (II) - обменялись своими ионами, т. е. произошла реакция обмена, уравнение которой:
Аналогично обмениваются ионами в результате реакции обмена иодид натрия и нитрат свинца (II) в растворе. В итоге выпадает жёлтый осадок иодида свинца (II) (рис. 109):

Рис. 109. Взаимодействие иодида натрия с нитратом свинца (II)
В демонстрационную пробирку нальём раствор щёлочи и добавим к нему несколько капель фенолфталеина. Содержимое пробирки окрасится в малиновый цвет, что свидетельствует о щелочной среде раствора. Если же теперь к содержимому пробирки прилить немного раствора кислоты, окраска исчезнет, раствор обесцветится, что является признаком химической реакции (рис. 110).

Рис. 110.
Взаимодействие растворов щёлочи и кислоты
Если несколько капель жидкости, полученной в результате реакции, выпарить на часовом стекле, то на нём образуются кристаллики соли. Ещё одним продуктом проведённой реакции является вода:
щёлочь + кислота → соль + вода.
Обратите внимание, взаимодействуют два сложных вещества: щёлочь, состоящая из ионов металла и гидроксид-ионов, и кислота - молекулярное соединение, которое в растворе образует ионы водорода и кислотного остатка. В итоге образуются два новых сложных вещества: ионное соединение - соль и молекулярное - вода.
В каждом из двух взаимодействующих растворов была своя среда, соответственно щелочная и кислотная. В результате реакции среда стала нейтральной. Поэтому реакцию обмена между кислотами и щелочами называют реакцией нейтрализации.
В демонстрационную пробирку нальём прозрачный бесцветный раствор карбоната натрия и добавим к нему немного раствора азотной кислоты. Признаком химической реакции послужит «вскипание» раствора из-за выделившегося в результате её углекислого газа (рис. 111):

Рис. 111.
Взаимодействие карбоната натрия с азотной кислотой
А откуда взялся углекислый газ? Вероятно, вы вспомните, что угольная кислота - непрочное соединение, которое распадается на углекислый газ и воду:
поэтому уравнение реакции следует записать так:
Сформулируем правило, согласно которому протекают реакции обмена между растворами веществ.
Если к раствору хлорида натрия прилить раствор гидроксида калия, то никаких признаков реакции нельзя будет заметить - реакция не идёт, так как в результате её не образуется ни осадка, ни газа, ни воды:
Ключевые слова и словосочетания
- Реакции обмена.
- Реакции нейтрализации.
- Условия протекания реакций обмена в растворах до конца.
Работа с компьютером
- Обратитесь к электронному приложению. Изучите материал урока и выполните предложенные задания.
- Найдите в Интернете электронные адреса, которые могут служить дополнительными источниками, раскрывающими содержание ключевых слов и словосочетаний параграфа. Предложите учителю свою помощь в подготовке нового урока - сделайте сообщение по ключевым словам и словосочетаниям следующего параграфа.
Вопросы и задания
ОПРЕДЕЛЕНИЕ
Химическими реакция называют превращения веществ, в которых происходит изменение их состава и (или) строения.
Наиболее часто под химическими реакциями понимают процесс превращения исходных веществ (реагентов) в конечные вещества (продукты).
Химические реакции записываются с помощью химических уравнений, содержащих формулы исходных веществ и продуктов реакции. Согласно закону сохранения массы, число атомов каждого элемента в левой и правой частях химического уравнения одинаково. Обычно формулы исходных веществ записывают в левой части уравнения, а формулы продуктов – в правой. Равенство числа атомов каждого элемента в левой и правой частях уравнения достигается расстановкой перед формулами веществ целочисленных стехиометрических коэффициентов.
Химические уравнения могут содержать дополнительные сведения об особенностях протекания реакции: температура, давление, излучение и т.д., что указывается соответствующим символом над (или «под») знаком равенства.
Все химические реакции могут быть сгруппированы в несколько классов, которым присущи определенные признаки.
Классификация химических реакций по числу и составу исходных и образующихся веществ
Согласно этой классификации, химические реакции подразделяются на реакции соединения, разложения, замещения, обмена.
В результате реакций соединения из двух или более (сложных или простых) веществ образуется одно новое вещество. В общем виде уравнение такой химической реакции будет выглядеть следующим образом:
Например:
СаСО 3 + СО 2 + Н 2 О = Са(НСО 3) 2
SO 3 + H 2 O = H 2 SO 4
2Mg + O 2 = 2MgO.
2FеСl 2 + Сl 2 = 2FеСl 3
Реакции соединения в большинстве случаев экзотермические, т.е. протекают с выделением тепла. Если в реакции участвуют простые вещества, то такие реакции чаще всего являются окислительно-восстановительными (ОВР), т.е. протекают с изменением степеней окисления элементов. Однозначно сказать будет ли реакция соединения между сложными веществами относиться к ОВР нельзя.
Реакции, в результате которых из одного сложного вещества образуется несколько других новых веществ (сложных или простых) относят к реакциям разложения . В общем виде уравнение химической реакции разложения будет выглядеть следующим образом:
Например:
CaCO 3 CaO + CO 2 (1)
2H 2 O =2H 2 + O 2 (2)
CuSO 4 × 5H 2 O = CuSO 4 + 5H 2 O (3)
Cu(OH) 2 = CuO + H 2 O (4)
H 2 SiO 3 = SiO 2 + H 2 O (5)
2SO 3 =2SO 2 + O 2 (6)
(NH 4) 2 Cr 2 O 7 = Cr 2 O 3 + N 2 +4H 2 O (7)
Большинство реакций разложения протекает при нагревании (1,4,5). Возможно разложение под действием электрического тока (2). Разложение кристаллогидратов, кислот, оснований и солей кислородсодержащих кислот (1, 3, 4, 5, 7) протекает без изменения степеней окисления элементов, т.е. эти реакции не относятся к ОВР. К ОВР реакциям разложения относится разложение оксидов, кислот и солей, образованных элементами в высших степенях окисления (6).
Реакции разложения встречаются и в органической химии, но под другими названиями — крекинг (8), дегидрирование (9):
С 18 H 38 = С 9 H 18 + С 9 H 20 (8)
C 4 H 10 = C 4 H 6 + 2H 2 (9)
При реакциях замещения простое вещество взаимодействует со сложным, образуя новое простое и новое сложное вещество. В общем виде уравнение химической реакции замещения будет выглядеть следующим образом:
Например:
2Аl + Fe 2 O 3 = 2Fе + Аl 2 О 3 (1)
Zn + 2НСl = ZnСl 2 + Н 2 (2)
2КВr + Сl 2 = 2КСl + Вr 2 (3)
2КСlO 3 + l 2 = 2KlO 3 + Сl 2 (4)
СаСО 3 + SiO 2 = СаSiO 3 + СО 2 (5)
Са 3 (РО 4) 2 + ЗSiO 2 = ЗСаSiO 3 + Р 2 О 5 (6)
СН 4 + Сl 2 = СН 3 Сl + НСl (7)
Реакции замещения в своем большинстве являются окислительно-восстановительными (1 – 4, 7). Примеры реакций разложения, в которых не происходит изменения степеней окисления немногочисленны (5, 6).
Реакциями обмена называют реакции, протекающие между сложными веществами, при которых они обмениваются своими составными частями. Обычно этот термин применяют для реакций с участием ионов, находящихся в водном растворе. В общем виде уравнение химической реакции обмена будет выглядеть следующим образом:
АВ + СD = АD + СВ
Например:
CuO + 2HCl = CuCl 2 + H 2 O (1)
NaOH + HCl = NaCl + H 2 O (2)
NаНСО 3 + НСl = NаСl + Н 2 О + СО 2 (3)
AgNО 3 + КВr = АgВr ↓ + КNО 3 (4)
СrСl 3 + ЗNаОН = Сr(ОН) 3 ↓+ ЗNаСl (5)
Реакции обмена не являются окислительно-восстановительными. Частный случай этих реакций обмена -реакции нейтрализации (реакции взаимодействия кислот со щелочами) (2). Реакции обмена протекают в том направлении, где хотя бы одно из веществ удаляется из сферы реакции в виде газообразного вещества (3), осадка (4, 5) или малодиссоциирующего соединения, чаще всего воды (1, 2).
Классификация химических реакций по изменениям степеней окисления
В зависимости от изменения степеней окисления элементов, входящих в состав реагентов и продуктов реакции все химические реакции подразделяются на окислительно-восстановительные (1, 2) и, протекающие без изменения степени окисления (3, 4).
2Mg + CO 2 = 2MgO + C (1)
Mg 0 – 2e = Mg 2+ (восстановитель)
С 4+ + 4e = C 0 (окислитель)
FeS 2 + 8HNO 3 (конц) = Fe(NO 3) 3 + 5NO + 2H 2 SO 4 + 2H 2 O (2)
Fe 2+ -e = Fe 3+ (восстановитель)
N 5+ +3e = N 2+ (окислитель)
AgNO 3 +HCl = AgCl ↓ + HNO 3 (3)
Ca(OH) 2 + H 2 SO 4 = CaSO 4 ↓ + H 2 O (4)
Классификация химических реакций по тепловому эффекту
В зависимости от того, выделяется ли или поглощается тепло (энергия) в ходе реакции, все химические реакции условно разделяют на экзо – (1, 2) и эндотермические (3), соответственно. Количество тепла (энергии), выделившееся или поглотившееся в ходе реакции называют тепловым эффектом реакции. Если в уравнении указано количество выделившейся или поглощенной теплоты, то такие уравнения называются термохимическими.
N 2 + 3H 2 = 2NH 3 +46,2 кДж (1)
2Mg + O 2 = 2MgO + 602, 5 кДж (2)
N 2 + O 2 = 2NO – 90,4 кДж (3)
Классификация химических реакций по направлению протекания реакции
По направлению протекания реакции различают обратимые (химические процессы, продукты которых способны реагировать друг с другом в тех же условиях, в которых они получены, с образованием исходных веществ) и необратимые (химические процессы, продукты которых не способны реагировать друг с другом с образованием исходных веществ).
Для обратимых реакций уравнение в общем виде принято записывать следующим образом:
А + В ↔ АВ
Например:
СН 3 СООН + С 2 Н 5 ОН↔ Н 3 СООС 2 Н 5 + Н 2 О
Примерами необратимых реакций может служить следующие реакции:
2КСlО 3 → 2КСl + ЗО 2
С 6 Н 12 О 6 + 6О 2 → 6СО 2 + 6Н 2 О
Свидетельством необратимости реакции может служить выделение в качестве продуктов реакции газообразного вещества, осадка или малодиссоциирующего соединения, чаще всего воды.
Классификация химических реакций по наличию катализатора
С этой точи зрения выделяют каталитические и некаталитические реакции.
Катализатором называют вещество, ускоряющее ход химической реакции. Реакции, протекающие с участием катализаторов, называются каталитическими. Протекание некоторых реакций вообще невозможно без присутствия катализатора:
2H 2 O 2 = 2H 2 O + O 2 (катализатор MnO 2)
Нередко один из продуктов реакции служит катализатором, ускоряющим эту реакцию (автокаталитические реакции):
MeO+ 2HF = MeF 2 + H 2 O, где Ме – металл.
Примеры решения задач
ПРИМЕР 1